Neben den klassischen Erregern wie T. rubrum rücken immer mehr neue Pilze aus aller Welt in den Fokus der hausärztlichen Praxis. Das gilt insbesondere für Dermatophyten, die Hautpilze. Sie stammen aus drei Gattungen: Trichophyton, Microsporum, Epidermophyton. Einige von ihnen sind hochkontagiös, mitunter hoch virulent, andere wiederum können Eiter bilden [2].
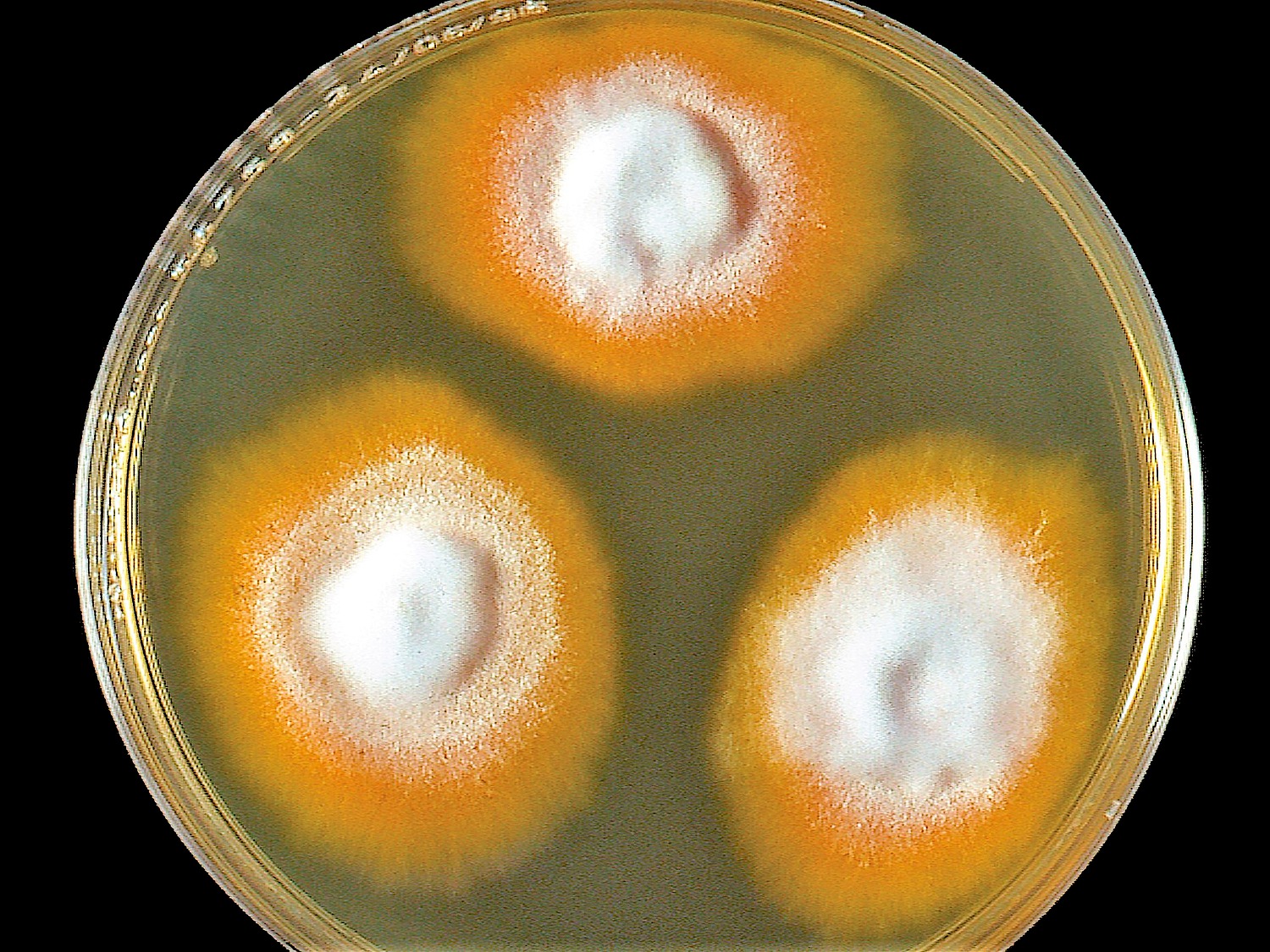
Trichophyton soudanense
Der aprikosen-farbige Erreger ist ein Paradebeispiel dafür, dass es heute keine geografisch streng lokalisierten Dermatophyten mehr gibt. Betroffen sind vor allem Kinder von Migranten aus Afrika.
Sporadische Infektionen gab es jedoch bereits in der DDR, was zeigt, dass auch Pilzerreger keine Mauern kennen [3] und der Keim aufgrund der mikrobiellen Globalisierung nicht mehr nur in Ländern wie im Sudan zu Hause ist, woher sein Name stammt (Abb. 1a unten).